酸性化合物の化学種のモル分率とpHとの関係 83回薬剤師国家試験問15
第83回薬剤師国家試験 問15
下の図はある酸性化合物の化学種(イオン形又は分子形)のモル分率とpHとの関係を示したものである。次の記述 a 〜 c の正誤を判定してみよう。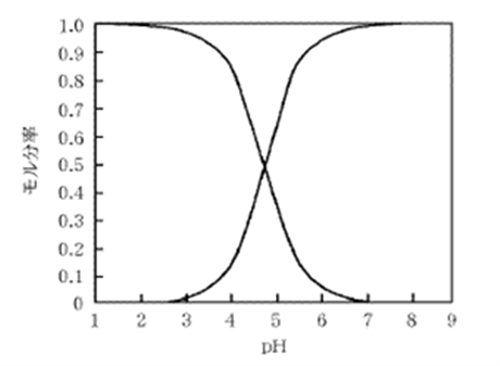
a 曲線の交点のpHは、その化合物のpKaに等しい。
b 曲線の交点より低いpHでは、イオン形の濃度が分子形の濃度より高い。
c pH 8以上ではほぼ完全に分子形として存在する。
第83回薬剤師国家試験 問15 解答解説
弱酸性薬物におけるpHの変化に対する各化学種(分子形・イオン形)の存在割合(存在比・分率)の変化についての問題である。
弱酸性物質におけるpHの変化に対する分子形・イオン形の存在比の変化の解説 へ
のモル分率とpHとの関係.jpg)
a 〇 曲線の交点のpHは、その化合物のpKaに等しい。
曲線の交点では、分子形とイオン形のモル分率が0.5となっている。
これは分子形とイオン形の分率が50%ずつであることを示す(分子形とイオン形の存在比が1:1であることを示す)。
よって、曲線の交点のpHは弱酸性化合物のpKaに等しい。
b × 曲線の交点より低いpHでは、イオン形の濃度が分子形の濃度より高い。
→ 〇 曲線の交点より低いpHでは、分子形の濃度がイオン形の濃度より高い。
→ 〇 曲線の交点より高いpHでは、イオン形の濃度が分子形の濃度より高い。
c × pH 8以上ではほぼ完全に分子形として存在する。
→ 〇 pH 8以上ではほぼ完全にイオン形として存在する。
→ 〇 pH 2以下ではほぼ完全に分子形として存在する。
弱酸性化合物においては、
pHがpKa−2より小さい値では(pH≦pKa−2)、99%以上が分子形(HA)として存在し、
pHがpKa+2より大きい値では(pH≧pKa+2)、99%以上がイオン形(A−)として存在する。