アルコール 分子間脱水でエーテル生成 反応機構 90回薬剤師国家試験問12c
90回薬剤師国家試験 問12c
下記のエーテルの合成法において、目的とするエーテルが主生成物として得られるか判定してみよう。
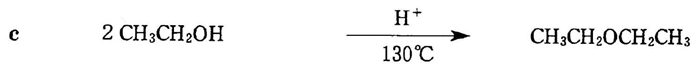
90回薬剤師国家試験 問12c 解答解説
設問の反応は第1級アルコールの酸性条件下での分子間脱水であり、図の構造のエーテルが主生成物として得られる。
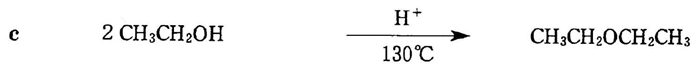
設問の反応は第1級アルコールの酸性条件下での分子間脱水である。
第1級アルコールを酸性条件下で130℃位に加熱すると、2分子のアルコールで分子間脱水反応が起こる。その結果、2つのアルコール分子が脱水縮合したエーテルを生成する。
アルコールの分子間脱水は、以下で示すようにSN2反応の機構で進行する。
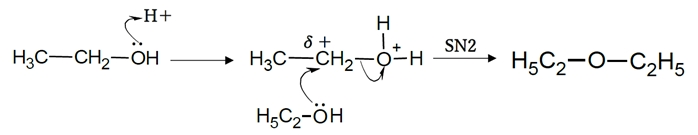
アルコールの酸性条件下での分子間脱水反応は、
始めにアルコールのヒドロキシ基が、酸によってプロトン化され、H2O+なる。
この変化は、以下で述べる2点からSN2の反応性を高める。
1つ目は、ヒドロキシ基が脱離しやすくなることである。
ヒドロキシ基は、そのまま脱離すると、安定性の低いOH−となるので、そのままでは脱離しにくい。
しかし、ヒドロキシ基が酸によってプロトン化され、
H2O+となると、安定なH2Oとなって脱離しやすくなる。
2つ目は、炭素が求核攻撃を受けやすくなることである。
ヒドロキシ基がH2O+になると、O +が共有電子対をより強く引っ張るようになり、H2O+が結合する炭素の正電荷(δ+)が大きくなるので、求核剤との反応性が高くなる。
アルコールの分子間脱水反応は、SN2反応の機構で起こるため、
1級アルコールのように反応中心炭素の立体障害が小さいアルコールでしか起こらない。
2級・3級アルコールのように反応中心炭素の立体障害が大きい基質では、分子間脱水は起こりにくい。
代わりに、2級・3級アルコールは、E1反応の機構で進行する分子内脱水が起こりやすい。
アルコールの分子内脱水については下記のリンク先を参照
アルコール 分子内脱水でアルケン生成 反応機構 89回問9a