標準酸化還元電位(標準電極電位)とは
本ページでは、標準酸化還元電位(標準電極電位)について説明しています。
電極電位(酸化還元電位)とは、
ある酸化還元反応系における電子のやり取りの際に発生する電位のことである。
電極電位は直接測定できない。
そこで、
電池の起電力 = 片方の電極の電位 − もう片方の電極の電位
であることを利用し、
測定対象電極と基準電極(参照電極)とで構成される電池の起電力を測定し、
基準電極の電極電位を0Vとすることで、
この電池の起電力を測定対象電極の電極電位とする。
このように電極電位は基準電極に対する相対値で表される。
標準電極電位(標準酸化還元電位)とは、
基準電極に標準水素電極を用い、
気体水素の圧力が1atmで、
電池内での酸化還元反応に関わる全ての化学種の活量が1という条件で算出された電極電位である。
下記は標準水素電極の模式図である。
水素電極の酸化還元反応は下記の通りである。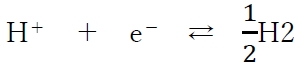
この酸化還元反応の標準酸化還元電位を0Vとする。
★ 参考外部サイトリンク
電位とは何?(電池の情報サイトさん)