水溶液中のイオン間相互作用 101回薬剤師国家試験問94の2,3,4
101回薬剤師国家試験 問94の2,3,4
水溶液中のイオン間相互作用に関する記述の正誤を判定してみよう。
2 難溶解性塩であるAgClの溶解度は、NaNO3の添加によるイオン強度の増大とともに増大する。
3 高濃度の強電解質溶液におけるイオンの平均活量係数は、1より大きくなることがある。
4 水中における電解質のイオン間相互作用は、アルコールなどを添加して溶媒の誘電率が低下すると減少する。
101回薬剤師国家試験 問94の2,3,4の解説
◆ 2について
2 〇 難溶解性塩であるAgClの溶解度は、NaNO3の添加によるイオン強度の増大とともに増大する。
難溶性塩の溶解度について、溶液中に難溶性塩と無関係なイオンが多量に存在すると、
難溶性塩の溶解度が増加する現象を、異種イオン効果と呼ぶ。
難溶性塩AgClの沈殿が存在する飽和溶液に、NaNO3を添加することを考える。
この添加により、AgClが解離して生成するイオン(Ag+とCl−)とは無関係な、
Na+とNO3−という異種イオンが多量に存在するようになると、
溶液のイオン強度が増大し、Ag+とCl−の平均活量係数が1より小さくなり、
AgClの溶解度が増大する。
あるイオンを中心に、それと反対符号を持つイオンが取り囲む構造をイオン雰囲気と呼ぶ。
異種イオンの添加により、溶液のイオン強度が増大すると、イオン雰囲気が増大し、
Ag+とCl−の結合が妨げられ、
難溶性のAgClの沈殿生成が抑えられるため、
AgClの溶解度が上昇すると考えられる。
関連問題
・93回問19bc
→ 共通イオン効果・異種イオン効果について解説
◆ 3について
3 〇 高濃度の強電解質溶液におけるイオンの平均活量係数は、1より大きくなることがある。
電解質の希薄溶液では、イオン強度が増大すると、イオン間の相互作用が強くなるため、イオンの平均活量係数は1 より小さくなる。
ただ、高濃度の強電解質溶液におけるイオンの平均活量係数は、1より大きくなることがある。これについて、高濃度ではイオンと溶媒分子との相互作用の影響が大きくなることが要因の1つと考えられている。
◆ 4について
4 × 水中における電解質のイオン間相互作用は、アルコールなどを添加して溶媒の誘電率が低下すると減少する。
→ 〇 水中における電解質のイオン間相互作用は、溶媒の誘電率が低下すると増大する。
陽イオンと陰イオンはクーロン力(F)という引力で結合している。
誘電率εの媒質中において2つの電荷QとQ´が距離r 離れているとき、この2つの電荷間に働くクーロン力(F)は次式で表される。
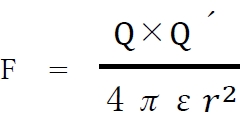
式より、溶媒の誘電率εが大きいほどクーロン力は小さくなり、溶媒の誘電率εが小さいほどクーロン力は大きくなることがわかる。
よって、誘電率εの大きい水に相対的に誘電率の小さいアルコールを混ぜて溶媒の誘電率を小さくすると、クーロン力は大きくなる。
関連問題
・106回問5
→ イオン間にはたらくクーロン力の特徴を解説