反応の進行に伴うエネルギー変化 91回薬剤師国家試験問21
91回薬剤師国家試験 問21
反応の進行に伴うエネルギー変化に関する記述の正誤について、正しいものはどれか。

a 反応速度定数kがアレニウスの式に従う場合、kと活性化エネルギーEaは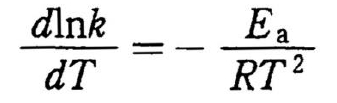
で関係づけられる。
b Eaの値は、0、1、2次反応のいずれの場合でも、反応速度定数と反応温度との関係式から求めることができる。
c 反応熱 ΔHの値が大きいほど、その平衡状態は反応温度の低下と共に反応前の系に傾く。
d 標準自由エネルギーが反応前より反応後の系で小さい場合、平衡は反応前の系に傾いている。
薬剤師国家試験過去問題集 アレニウス式・エネルギー図 一覧へ
91回薬剤師国家試験 問21 解答解説

◆ a,bについて
a × 反応速度定数kがアレニウスの式に従う場合、kと活性化エネルギーEaは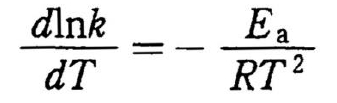
で関係づけられる。
b 〇 Eaの値は、0、1、2次反応のいずれの場合でも、反応速度定数と反応温度との関係式から求めることができる。
詳細は下記のリンク先を参照
アレニウス式 反応速度定数と反応温度との関係式 91回問21ab
◆ cについて
c × 反応熱ΔHの値が大きいほど、その平衡状態は反応温度の低下と共に反応前の系に傾く。
→ 〇 反応熱ΔHの値が大きいほど、その平衡状態は反応温度の低下と共に反応後の系に傾く。
詳細は下記のリンク先を参照
91回問21c
◆ dについて
d × 標準自由エネルギーが反応前より反応後の系で小さい場合、平衡は反応前の系に傾いている。
→ 〇 標準自由エネルギーが反応前より反応後の系で小さい場合、平衡は反応後の系に傾いている。
自発的な変化において、
系はギブズエネルギー(G)の小さくなる方向へと進む。
よって、標準ギブズエネルギーが反応前より反応後の系で小さい場合、
自発的な変化は反応後の系になる方向に傾く。