tolueneの環炭素とメチル基シグマの結合 87回薬剤師国家試験問6a
第87回薬剤師国家試験 問6
原子の軌道に関する下記の記述の正誤を判定してみよう。
a tolueneの環炭素とメチル基との結合は、p軌道とsp3混成軌道とからなるパイ(π)結合である。
第87回薬剤師国家試験 問6 解答解説
◆ aについて
a × tolueneの環炭素とメチル基との結合は、p軌道とsp3混成軌道とからなるパイ(π)結合である。
→ 〇 tolueneの環炭素とメチル基との結合は、環炭素のsp2混成軌道とメチル基の炭素のsp3混成軌道とからなるシグマ(σ)結合である。
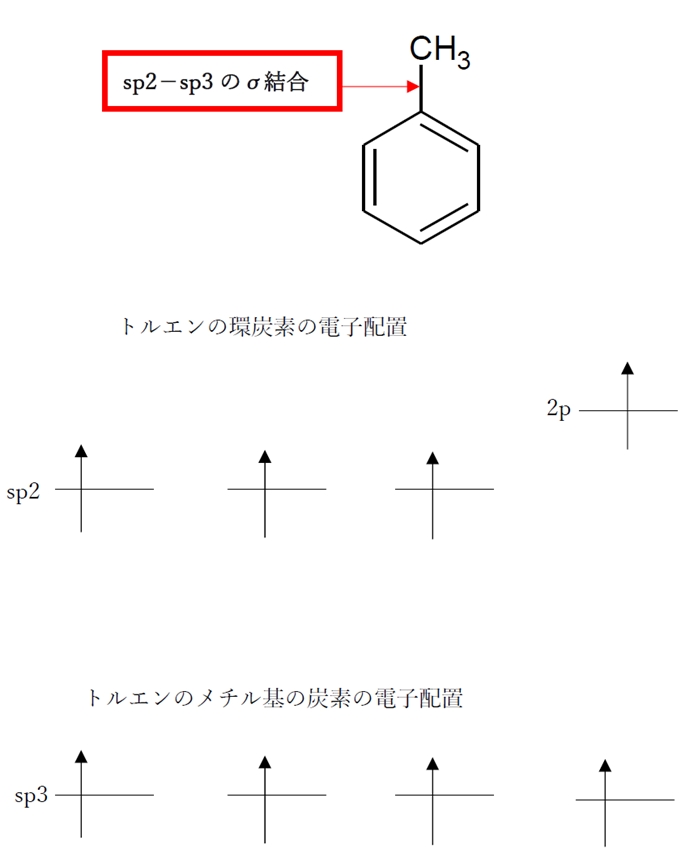
なお、2つの原子間が1つまたは複数共有結合を形成している時、必ずそのうちのどれか1つだけはσ結合であり、単結合の場合はその結合は必ずσ結合である。
◆ bについて
b 〇 ammonia窒素の非共有電子対はsp3混成軌道を占めるのに対し、pyridine窒素の非共有電子対はsp2混成軌道を占めている。

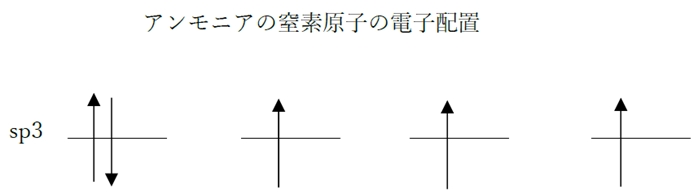
ピリジンについては、下記のリンク先を参照
ピリジンとピロール 非共有電子対の軌道 88回問8c
◆ cについて
c 〇 ethylene(ethene)炭素の混成軌道はsp2であるのに対し、acetylene(ethyne)炭素の混成軌道はspであり、後者の方が混成軌道のs性が高い。
下記のリンク先を参照
エチレン,アセチレンの混成軌道と酸性度 82回問2cd
◆ dについて
d × 第2周期の元素にはすべて、2s、2p、2d軌道に電子が存在する。
第2周期のうち、LiとBeの最外殻電子は2s軌道に入り、
B、C、N、O、F、Neの最外殻電子は2s軌道と2p軌道に入っている。
なお、2d軌道という軌道はない。