患者の体液中のHCO3-/H2CO3の存在比に最も近い値はどれか 102回薬剤師国家試験問97
第102回薬剤師国家試験 問97
ヒトの体液は主に炭酸と炭酸水素イオンの濃度バランスによりpH 7.4に維持されている。
pH 7.3のアシドーシスを起こした患者の体液中のHCO3-/H2CO3の存在比に最も近い値はどれか。1つ選びなさい。
ただし、炭酸は次式のように解離し、その2つのpkaは、それぞれpKa1= 6.1、pKa2= 10.5とする。
またlog1.6=0.2とする。
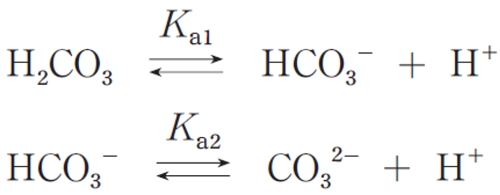
1 1.6
2 2.0
3 8.3
4 16
5 20
第102回薬剤師国家試験 問97 解答解説
正解は4の16である。
互いに共役である酸(acid)と塩基(base)の対をそれぞれある濃度以上含む水溶液を緩衝液という。
緩衝液では、外部から酸や塩基が加わることに対してpHの変動を抑制する緩衝作用が働く。
酸をHA,その共役塩基をA-とすると、HAとA-の酸塩基反応は便宜的に次のように表される。
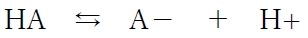
この酸塩基反応の平衡定数をHAの酸解離定数Kaとすると、
酸HAとその共役塩基A-について、次のヘンダーソン・ハッセルバルヒの式が成り立つ。
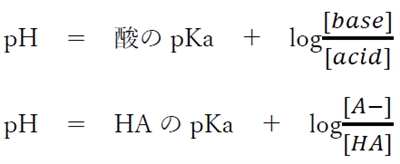
これを変形すると、
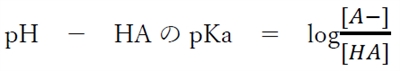
これより、pHとHAのpKaの差がわかれば、 HAとA-の濃度比(存在比)を求めることができる。
本問では、体液のpHを一定に保つのに重要な酸H2CO3とその共役塩基HCO3-による緩衝系を題材に、pH7.3におけるHCO3-/H2CO3の存在比を求める。
問題文より、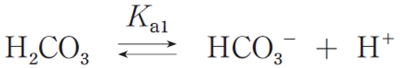
pKa1=6.1
なので、
H2CO3のpKa=6.1 である。
よって、ヘンダーソン・ハッセルバルヒの式を酸H2CO3とその共役塩基HCO-に適用すると次式が成り立つ。
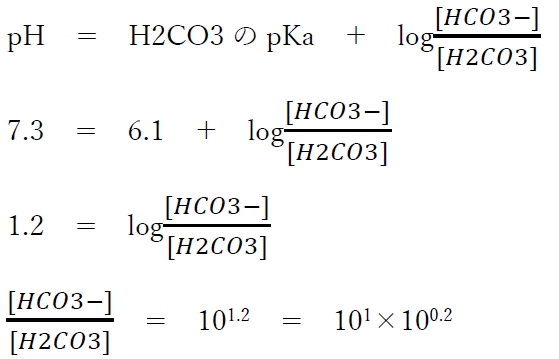
ここで、
log1.6=0.2 より、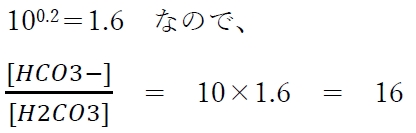
★参考外部サイトリンク
pHおよび解離定数(yakugaku labさん)
★他サイトさんの解説へのリンク
102回問97(e-RECさん)