相平衡・相の安定性と化学ポテンシャル 102回薬剤師国家試験問93の1,3
102回薬剤師国家試験 問93の1,3
下図の実線はある純物質の化学ポテンシャルと温度の関係を示したグラフである。次の記述のうち、正しいのはどれか。2つ選びなさい。

1 このグラフの傾きはモルあたりのエントロピーを表す。
3 温度がT3のとき、液相よりも気相の化学ポテンシャルが高いため、この純物質は自発的に気相に変化する。
102回薬剤師国家試験 問93の1,3
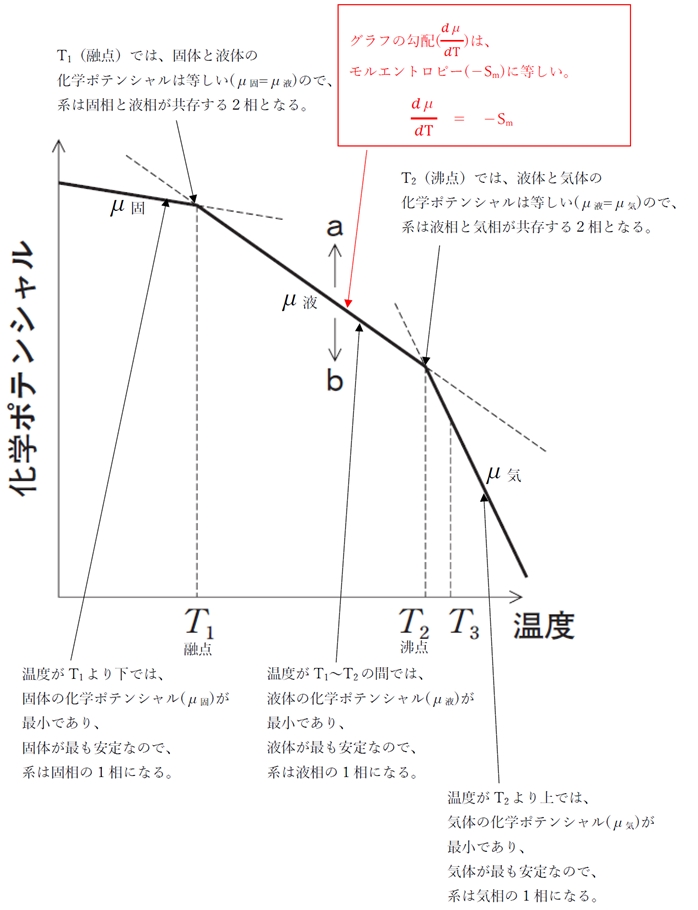
1 〇 このグラフの傾きはモルあたりのエントロピーを表す。
3 × 温度がT3のとき、液相よりも気相の化学ポテンシャルが高いため、この純物質は自発的に気相に変化する。
→ 〇 温度がT3のとき、液相よりも気相の化学ポテンシャルが低いため、この純物質は自発的に気相に変化する。
★ ギブズエネルギー(G)の温度依存性
閉鎖系においては、
系のギブズエネルギー(G)の温度・圧力依存性について、
次式が成り立つ。
dG = V・dp - S・dT …①
(dは微小変化を表す)
dG:ギブズエネルギーの微小変化
V:体積 dp:圧力の微小変化
S:エントロピー dT:温度の微小変化
定圧条件下では、dp=0であるので、
dG = -S・dT …②
となる。
②式より、
ギブズエネルギーは、圧力一定の条件下では温度の上昇に伴って増加するといえる。
②式を変形すると、次の③式となる。
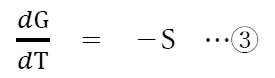
系が純物質(一成分系)の場合、
③式を1mol当たりの量で考えると、次の④式となる。
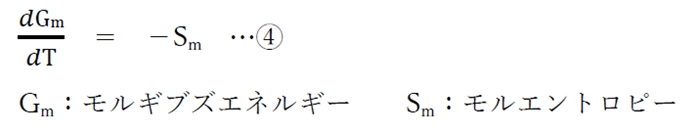
系が純物質(一成分系)の場合に限り、
モルギブズエネルギー = 化学ポテンシャル(μ:ミュー)
であるので、④式より、次の⑤式が成り立つ。
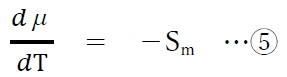
⑤式は
単位温度変化に対する化学ポテンシャルの変化は、
モルエントロピーに等しいことを示す。
設問の図は、純物質(一成分系)における、
温度と化学ポテンシャル(純物質ならモルギブズエネルギー)の関係を示す。
熱力学的に化学ポテンシャルの小さい方が安定である。
系は化学ポテンシャルの小さい状態になろうとするので、
温度変化に伴い、グラフの実線に沿って物理的状態が変化する。

なお、化学ポテンシャルは、本来、部分モルギブズエネルギーであることに注意する
(モルギブズエネルギーと部分モルギブズエネルギーは異なる)。
化学ポテンシャル = モルギブズエネルギー
が成り立つのは、系が純物質(一成分系)の場合に限定される。
化学ポテンシャルについては下記のリンク先を参照
化学プテンシャルとは