質量分析 塩素を含む場合の同位体ピーク
本ページでは、質量分析においてハロゲンの塩素Clを含む場合の同位体ピークについて説明しています。
◆ 塩素の同位体ピーク
塩素の同位体の天然存在比について、
35Clが約76%,37Clが約24%なので、
1つの塩素につき、
35Cl:37Cl = 約3:1
で存在する。
これを踏まえ、
塩素を1つ含む場合と2つ含む場合の同位体ピークについて述べる。
(1)塩素を1つ含む場合の同位体ピーク
含まれる塩素の同位体の確率は下記の通り。
35Clの確率=3/4
37Clの確率=1/4
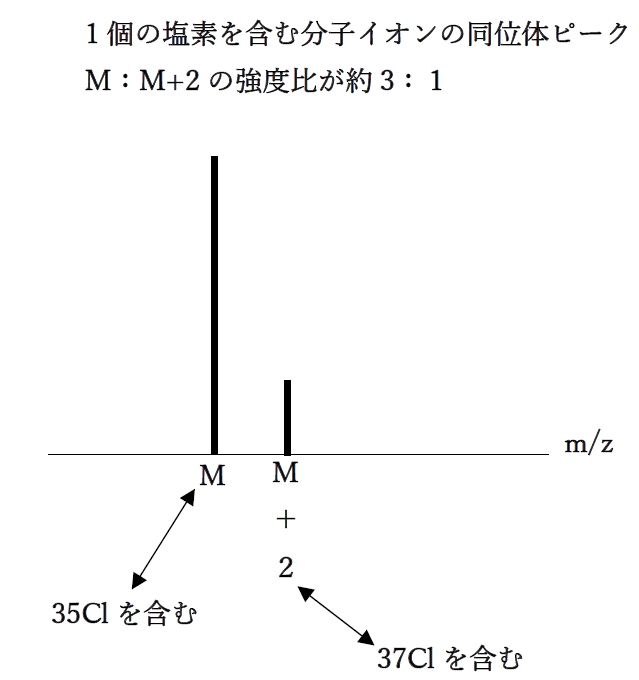
よって、1個の塩素を含む分子イオンは、
2マスユニット間隔で強度比が約3:1の2本のピークとして出現する。
(2)塩素を2つ含む場合の同位体ピーク
塩素の同位体の天然存在比より、
2つの塩素の同位体の組み合わせの確率は下記の通り。
35Cl−35Clの確率=3/4×3/4=9/16
35Cl−37Clの確率=3/4×1/4=3/16
37Cl−35Clの確率=1/4×3/4=3/16
37Cl−37Clの確率=1/4×1/4=1/16
35Cl−37Clと37Cl−35Clの質量は同じである。
よって、2個の塩素を含む分子イオンは、
2マスユニット間隔で強度比が約9:6:1の3本のピークとして出現する。

以上のようなピークのパターンが見られた場合、
試料は塩素を含む化合物であることが考えられる。
なお、臭素の同位体ピークについては下記のリンク先を参照
臭素の同位体ピーク