フェノールの定量法 反応式,対応量 102回薬剤師国家試験問96の1,2,3
102回薬剤師国家試験 問96の1,2,3
日本薬局方フェノール(C6H6O:94.11)の定量法に関する記述の正誤を判定してみよう。

1 A に入る試液は、ヨウ化カリウム試液である。
2 B の対応量は、4.705である。
3 下線においてクロロホルムを加える理由は、沈殿した2,4,6-トリブロモフェノールを溶解させるためである。
102回薬剤師国家試験 問96の1,2,3 解答解説
◆ 1,2,3について
1 〇 A に入る試液は、ヨウ化カリウム試液である。
2 × B の対応量は、4.705である。
→ 〇 B の対応量は、1.569である。
3 〇 下線においてクロロホルムを加える理由は、沈殿した2,4,6-トリブロモフェノールを溶解させるためである。
本問の定量法は、酸化還元平衡を定量に利用する酸化還元滴定である。
試料に一定過剰量の臭素液を加え、
試料中のフェノールとBr2を反応させ、2,4,6-トリブロモフェノールを生成する。
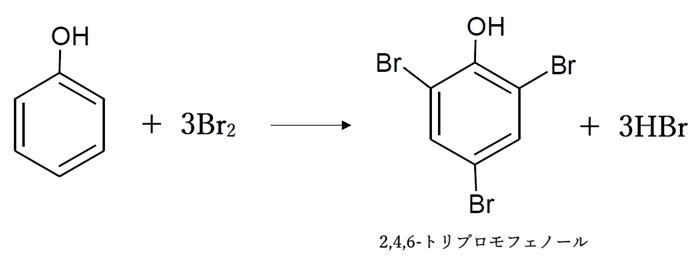
この反応で、1molのフェノールに対して3molのBr2が反応する。
過剰に加えた未反応の臭素Br2にヨウ化カリウム(KI)を加えると、
酸化剤としての強さは、Br2>I2であるため、
Br2がI-(ヨウ化物イオン)を酸化してI2を生成する。
Br2 + 2I- → 2Br + I2
この反応で、1molのBr2から1molのI2が生じる。
生成したI2をチオ硫酸ナトリウム液(Na2S2O3)で滴定する。
I2 + 2 S2O3 2- → 2I- + S4O6 2-
この反応で、1molのI2に対して2molのNa2S2O3が反応する。
この滴定では指示薬としてデンプン試液を用いる。
当量点前の未反応のI2が残存する間は、
I2とデンプンの電荷移動錯体により青紫色を呈する
(デンプンのらせん構造にI2が入り込む包接化合物を生じ青紫色を呈する)。
当量点に達し、未反応のI2が無くなると、
I2とデンプンの電荷移動錯体が無くなり、青紫色が消失する。
問題文の下線においてクロロホルムを加える理由は、
沈殿した2,4,6-トリブロモフェノールを溶解させるためであり、
これで終点がわかりやすくなる。
本定量法では臭素Br2をヨウ化物イオン(I-)で還元する過程を経る。
酸化還元滴定のうち、
本法のようにヨウ化物イオンを還元剤として用いる方法をヨードメトリー(ヨウ素還元滴定)と呼ぶ。
★ 0.05mol/L臭素液のフェノールの対応量
1molのフェノールに対して3molのBr2が反応する。
これに基づき、
0.05mol/L臭素液1mLのフェノールの対応量を求める。
0.05mol/L臭素液1mLに含まれる臭素は0.05mmolである。
0.05mmolの臭素は1/3×0.05mmolのフェノールに対応する。
本問ではフェノールの分子量を94.11とするので、
1/3×0.05mmolのフェノールの質量は、
1/3×0.05mmol×94.11 (g/mol)≒ 1.569mg
したがって、
0.05mol/L臭素液1mLのフェノールの対応量は下記の通り。
0.05mol/L臭素液1mL = 1.569mg フェノール
★ 式による対応量の計算
対応量(mg)は下記の計算式を用いても計算できる。

本問では、フェノールと臭素Br2の反応について、
フェノール(目的成分)の化学当量は1、
臭素(目的成分と反応する成分)の化学当量は3である。
臭素液の濃度は0.05mol/L、
フェノールの分子量は94.11であるので、
対応量(mg)は式を用いて下記のように計算できる。
