非水滴定 ブロムヘキシン塩酸塩の定量法 98回薬剤師国家試験問203
98回薬剤師国家試験 問203
日本薬局方ブロムヘキシン塩酸塩の定量法を以下に示す。□の中に入れるべき数値として、正しいのはどれか。1つ選びなさい。

1 20.63
2 41.26
3 82.52
4 103.1
5 206.3
98回薬剤師国家試験 問203 解答解説
正解は2の41.26である。
0.1mol/L過塩素酸液 = 41.26mg C14H20Br2N2・HCl
本定量法は、非水滴定である。
非水滴定とは、水以外の溶媒を用いて行う中和滴定(酸塩基滴定)である。
本定量法の中で、無水酢酸を加え、加温する操作がある。
酸無水物は求核剤と反応して、求核アシル置換反応を起こす。
ブロムヘキシンと無水酢酸を反応させると、
無水酢酸(酸無水物)に対してブロムヘキシンの芳香族第1級アミンが求核攻撃を行い、求核アシル置換反応の結果、アミドが生成する(芳香族第1級アミンはアセチル化される)。
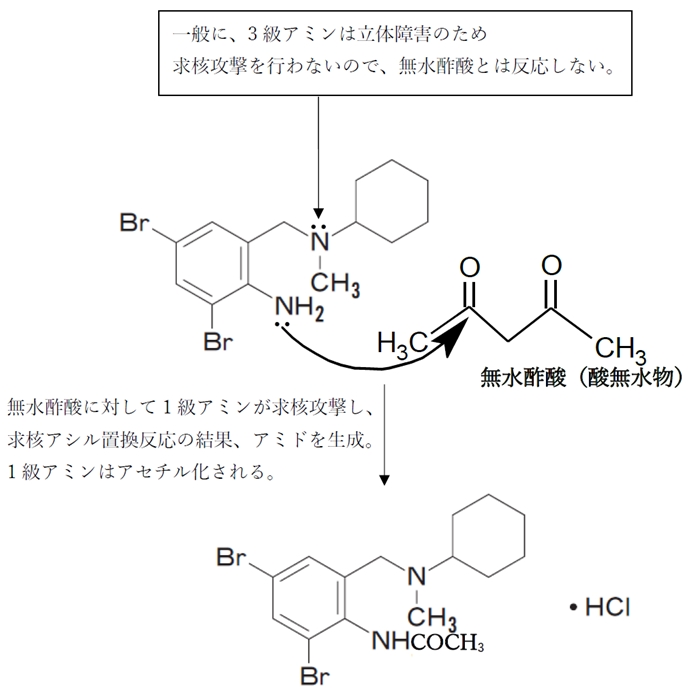
ブロムヘキシンには第3級アミンもあるが、
一般に、3級アミンは窒素周りの立体障害が大きいため求核反応を起こしにくいので、
ブロムヘキシンの3級アミンは酸無水物とは反応しない。
次に、
非水滴定の指示薬としてクリスタルバイオレットを用い、
0.1mol/L過塩素酸で滴定する。
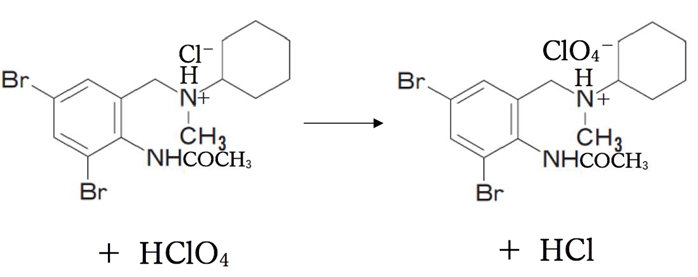
このように、
ブロムヘキシンの3級アミンの塩酸塩と過塩素酸(HClO4)がモル比1:1で対応する。
過塩素酸を用いる非水滴定では、
塩酸は追い出されるので、
塩酸の影響は考えなく良い。
上記に基づき、
0.1mol/L過塩素酸液1mLのブロムヘキシン塩酸塩の対応量を求める。
0.1mol/L過塩素酸液1mLに含まれる過塩素酸は0.1mmolである。
0.1mmolの過塩素酸は0.1mmolのブロムヘキシン塩酸塩に対応する。
本問ではブロムヘキシン塩酸塩の分子量を412.59とするので、
0.1mmolのブロムヘキシン塩酸塩の質量は、
0.1mmol×412.59 (g/mol) ≒ 41.26mg
したがって、
0.1mol/L過塩素酸液1mLのブロムヘキシン塩酸塩の対応量は下記の通り。
0.1mol/L過塩素酸液 = 41.26mg C14H20Br2N2・HCl
★ 捕捉:式による対応量の計算
対応量(mg)は下記の計算式を用いても計算できる。

本問では、ブロムヘキシン塩酸塩と過塩素酸の反応について、
ブロムヘキシン塩酸塩(目的成分)の化学当量は1、
過塩素酸(標準液の成分)の化学当量は1である。
過塩素酸液の濃度は0.1mol/L、
ブロムヘキシン塩酸塩の分子量は412.59であるので、
対応量(mg)は式を用いて下記のように計算できる。

★ 他サイトさんの解説リンク
98回問202,203(e-RECさん)