ピンドロールの合成法 第90回薬剤師国家試験問9
第90回薬剤師国家試験 問9
次の反応式は、日本薬局方医薬品ピンドロールの2つの合成法を示したものである。この合成法に関する記述の正誤を判定してみよう。ただし、図中の不斉炭素を有する化合物はすべてラセミ体である。

a 反応Aは、カルボニル炭素に対するアミンの求核置換反応である。
b 反応Cは、インドール環上のヒドロキシアニオンのエポキシドに対する求核的な反応である。
c エポキシドは、結合角によるひずみのため、通常のエーテルとは異なる反応性を示す。
d 反応Dでは、窒素原子とベンジル基の間の結合が還元的に開裂する。
第90回薬剤師国家試験 問9 解答解説
◆ aについて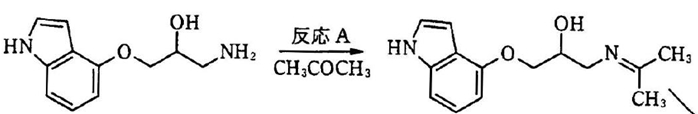
a × 反応Aは、カルボニル炭素に対するアミンの求核置換反応である。
→ 〇 反応Aは、カルボニル炭素に対するアミンの求核付加反応である。
一般に、アルデヒド・ケトンのカルボニル炭素に対する求核剤の反応は求核付加反応となる。
反応Aは、ケトンであるCH3COCH3の正に分極するカルボニル炭素に対し、
1級アミンが求核剤として付加し、その後の脱水を経て、
結果として、イミンが生成する求核付加反応である。

アルデヒド・ケトンとアミンの反応については下記のリンク先を参照
アルデヒド,ケトンと1級2級アミンの反応 89回問10d
◆ bについて

b ○ 反応Cは、インドール環上のヒドロキシアニオンのエポキシドに対する求核的な反応である。
反応Cは塩基性条件におけるエポキシド(オキシラン)の開環反応である。
エポキシド(オキシラン)開環反応は、塩基性条件下と酸性条件下とで反応機構が異なる。
詳細は下記のリンク先を参照
エポキシドの開環の反応機構 酸性と塩基性での違い
反応Cは下記のように進む。

◆ cについて
c ○ エポキシドは、結合角によるひずみのため、通常のエーテルとは異なる反応性を示す。
通常のエーテルの反応性は低く、エーテルのC−O−C結合は開裂しにくい。
しかし、環状エーテルであるエポキシド(オキシラン)は、結合角が60°であり、sp3の理想的の角度が109.5°から大きく解離しているため、結合角ひずみが生じており不安定である。
エポキシドは開環すれば結合角ひずみが解消されて安定性が高まるため、
エポキシドは通常のエーテルに比べて反応性が高い。
◆ dについて
d 〇 反応Dでは、窒素原子とベンジル基の間の結合が還元的に開裂する。

金属触媒下で水素を反応させる接触還元により、ベンジル位の炭素と窒素または酸素との結合を還元的に開裂することができる。
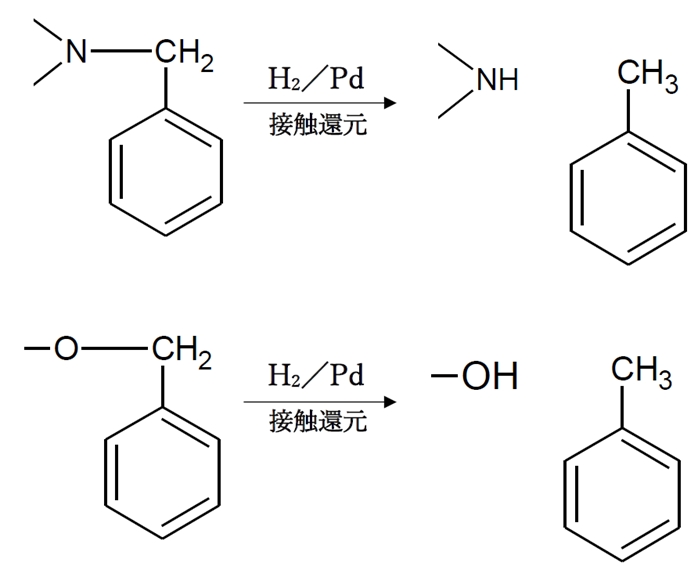
上記の反応は、ベンジル基を保護基として保護していたアミン・ヒドロキシ基を脱保護する反応となる。