98回薬剤師国家試験問8改題 反応分類
第98回薬剤師国家試験 問8改題※
下記の反応について、求核付加反応,求電子付加反応,求核置換反応,求電子置換反応,脱離反応のどれに該当するか判定してみよう。
なお、反応4はCH3Iを基質とする。
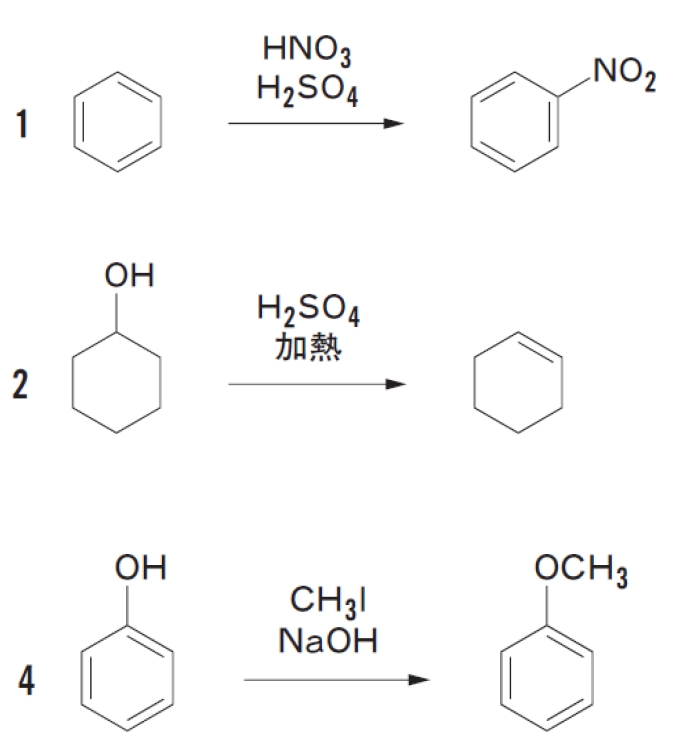
※ 本試験では選択肢3でディールスアルダー反応が出題されたが、新コアカリキュラムではディールスアルダー反応はアドバンストの内容と考えられたため、本ページでは割愛させていただいた。
第98回薬剤師国家試験 問8改題 解答解説
◆ 1について

反応1は芳香族化合物の求電子置換反応である。
芳香族求電子置換反応の反応機構については下記のリンク先を参照
芳香族化合物の求電子置換反応の反応機構 89回問5c
反応1は芳香族化合物の求電子置換反応によるニトロ化である。
発煙硝酸(濃硝酸の1種)と濃硫酸を反応させると、
硝酸が硫酸によりプロトン化され、
その後、脱水が起きてニトロニウムイオン(+NO2)を生成する。
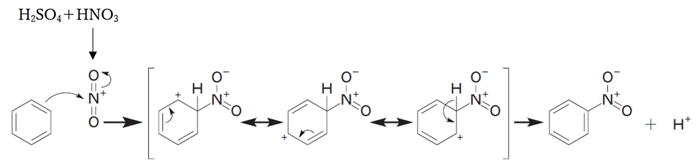
次いで、電子豊富な芳香環の1つの炭素に対して求電子剤のニトロニウムイオンが付加してカルボカチオン中間体を生成し、
次に同じ炭素から水素がプロトンとして外れ、
結果、芳香環の炭素の1つにおいて水素とNO2が置換したものが生成する
(求電子置換反応によるニトロ化)。
なお、芳香族求電子置換反応はスルホン化など一部を除きほとんどが不可逆反応である。
遷移状態のエネルギーの高さや中間体の安定性で反応速度が決まり、速度論的に進行する。
◆ 2について

反応2は、酸性条件下でのアルコールの分子内脱水であり、
OHとHが脱離してアルケンが生成しているので、脱離反応に該当する。
酸性条件下におけるアルコールの分子内脱水はE1脱離反応の機構で進行する。
詳細は下記のリンク先を参照
アルコールの酸性条件下での分子内脱水でアルケン生成 89回問9a
反応2のアルコールの酸性条件下での分子内脱水でアルケンを生成する反応(E1機構)は、下記のように進むと考えられる。

◆ 4について

反応4はSN2反応(二分子求核置換反応)であり、
ウイリアムソンのエーテル合成と呼ばれる。
ウイリアムソンのエーテル合成の詳細は下記のリンク先を参照
ウイリアムソンのエーテル合成 99回問103
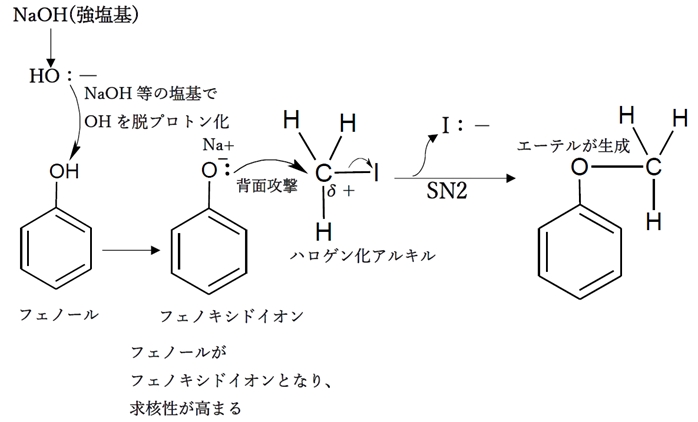
フェノールにNaOHのような強塩基を反応させると酸塩基反応によりフェノキシドイオン(Ph−O-)を生成し、
これが基質のハロゲン化アルキルのハロゲン−sp3炭素の正に分極したCδ+に対して求核攻撃すると同時にハロゲンが脱離し(SN2反応)、
結果、基質においてハロゲンとフェノキシド(Ph−O)が置換したエーテルが生成する。
反応4のSN2反応は、下記のように進むと考えられる。
★他サイトさんの解説へのリンク
第98回問8(e-RECさん)