一次速度式に従う反応 82回薬剤師国家試験問26
82回薬剤師国家試験 問26
物質Xが物質Yへと変化する反応が一次反応速度式に従うとする。この反応に関する次の記述の正誤について、正しいものはどれか。
a 反応速度はXの濃度とYの濃度との積に比例する。
b 反応温度を一定にしておけば、Xの半減期はXの初濃度には無関係である。
c 反応速度定数kの次元は(時間)-1となる。
d 反応速度定数kがArrhenius式k = A・exp(-E/RT)に従うとすれば、温度Tの上昇にともなってkは小さくなる。
82回薬剤師国家試験 問26 解答解説
設問の反応X→Yは一次反応速度式に従う
1次反応の特徴は下記のリンク先を参照
1次反応の速度式,半減期,グラフ
◆ aについて
a × 反応速度はXの濃度とYの濃度との積に比例する。
→ 〇 反応速度はXの濃度に比例する。
反応X→Yが一次反応に従う時、
一次反応の反応速度について、
微分型速度式として次の①式が成り立つ。

よって、
X→Yの反応速度は反応物Xの濃度に比例する。
◆ bについて
b 〇 反応温度を一定にしておけば、Xの半減期はXの初濃度には無関係である。
一次反応の反応物の半減期(t1/2)について次式が成り立つ。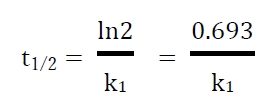
上式より、一次反応の反応物の半減期は、
反応物の初濃度(C0)とは無関係で一定であるといえる。
◆ cについて
c 〇 反応速度定数kの次元は(時間)-1となる。
反応速度定数kの次元を知るには、
微分型速度式をk=○○の式に変換すればよい。

よって、1次反応の反応速度定数(k1)の次元は、
時間-1である。
◆ dについて
d × 反応速度定数kがArrhenius式k = A・exp(-E/RT)に従うとすれば、温度Tの上昇にともなってkは小さくなる。
→ 〇 反応速度定数kがArrhenius式k = A・exp(-E/RT)に従うとすれば、温度Tの上昇にともなってkは大きくなる。
反応速度定数kと絶対温度Tの関係式として、
下記のアレニウス式がある。

アレニウス式より、反応速度定数kは温度の上昇とともに指数関数的に上昇する。
また、反応速度定数kは頻度因子(A)とexp(-Ea/RT )に比例するともいえる。