91回薬剤師国家試験問165 1次反応に従った薬物の分解
91回薬剤師国家試験 問165
薬物Aの水溶液中(初濃度40 mg/mL)での分解過程について、時間(hr)に対して濃度C(mg/mL)の常用対数値をプロットしたところ、下のグラフのようになった。次の記述の正誤について、正しいものはどれか。

a 分解は0次反応速度式に従っている。
b 反応の半減期は約8時間である。
c 反応速度定数は、0.1 hr-1である。
d 反応開始から20時間後には、薬物Aの約99%が分解することが予測される。
91回薬剤師国家試験 問165 解答解説
◆ aについて
a × 分解は0次反応速度式に従っている。
→ 〇 分解は1次反応速度式に従っている。
時間に対して濃度の対数をプロットしたグラフが直線を描いているので、
薬物Aの分解は一次反応速度式に従っていると考えられる。
1次反応については下記のリンク先を参照
1次反応の特徴 速度式,半減期,グラフ
◆ b,cについて
b × 反応の半減期は約8時間である。
→ 〇 反応の半減期は約6時間である。
c × 反応速度定数は、0.1 hr-1である。
→ 〇 反応速度定数は、0.23 hr-1である。
薬物Aの分解は一次反応に従うことから、
時間と濃度の常用対数の関係式として、
次式が成り立つ。

これより、
設問のグラフの傾きは-k1/2.303である(k1は一次反応速度定数)。
よって、グラフより、
傾きと速度定数k 1について次式が成り立つ。
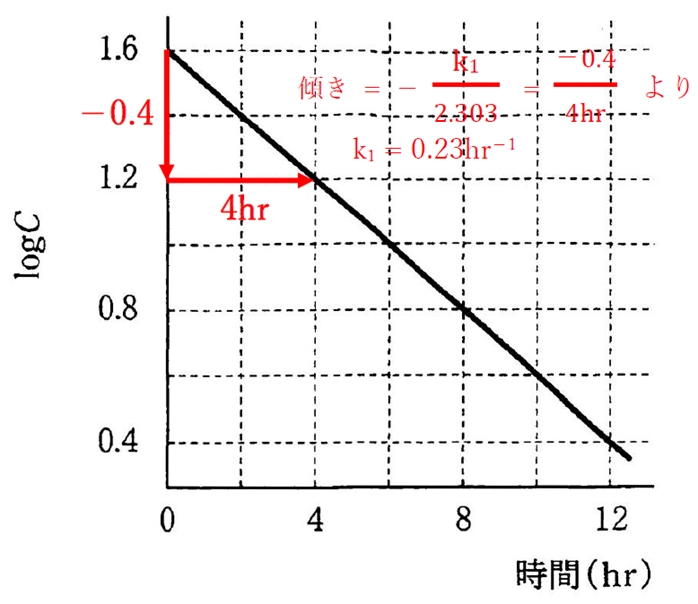
よって、
k1 = 0.23hr-1と求まる。
分解が一次反応に従う場合、
半減期について次式が成り立つ。

〈別解〉
グラフより、
縦軸の値が1.6から1.0になるのに6時間であることから、
濃度Cが初濃度の40 mg/mLから10 mg/mLになるのに6時間だとわかる。

分解が一次反応に従う場合、
半減期は濃度によらず一定なので、
濃度が1/4 = (1/2) 2 になるのに6時間要したことから、
半減期は3時間だとわかる。
分解が一次反応に従う場合、
半減期について次式が成り立つ。

◆ dについて
d 〇 反応開始から20時間後には、薬物Aの約99%が分解することが予測される。
薬物Aの分解は一次反応に従うことから、
時間と濃度の常用対数の関係式として、
次の①式が成り立つ。
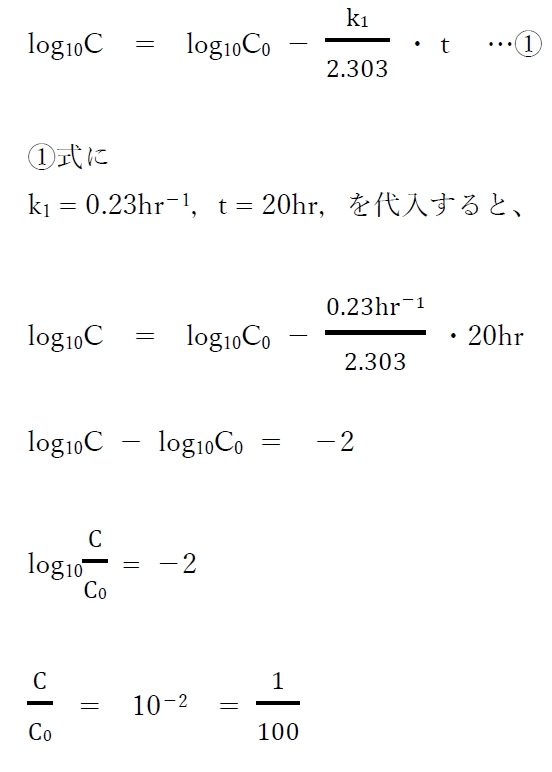
よって、反応開始から20時間後には、
薬物Aの濃度は初期濃度の1/100になる。
以上より、
反応開始から20時間後には、
薬物Aの約99%が分解することが予測されるといえる。